Некрасова Елизавета Георгиевна
К.м.н., врач-дерматоловенеролог, трихолог, доцент кафедры дермато-венерологии и косметологии, Тверь
Давидян Ованес Вагенович
Врач-терапевт, генеральный директор «ОДАС Фарма», член Ассоциации междисциплинарной медицины, Москва
Иванова Анастасия Сергеевна
Врач-трихолог, Тверь
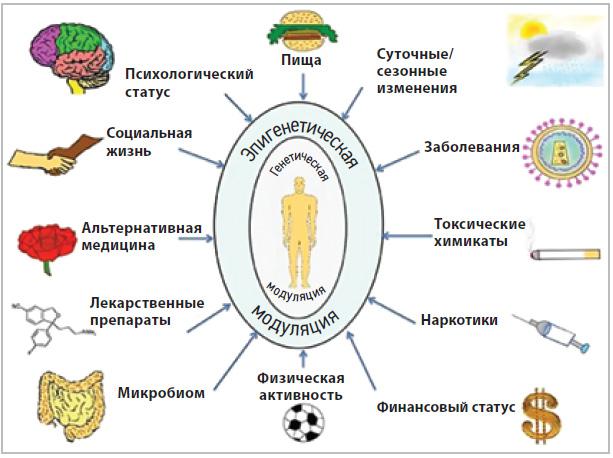
Эпигенетика может играть важную роль в развитии заболеваний человека. По образному выражению Питера и Джин Медаваров, «генетика предполагает, а эпигенетика располагает» [1]. Полиморфизм генов предрасположенности в сочетании с неблагоприятными внутренними и внешними факторами повышает риск развития заболеваний. К числу важнейших факторов, влияющих на эпигеном, относятся питание, физическая активность, неблагоприятная экология, ионизирующая радиация и др. Сбалансированный пищевой рацион и рациональная нутрициональная поддержка помогают укрепить собственные защитные силы организма, повысить его сопротивляемость и репаративный потенциал в т.ч. за счет эпигенетической модуляции работы клеточного генома.
Ключевые слова: эпигенетика, нутрициональная поддержка, омега-3 полиненасыщенные жирные кислоты, витамин D
Кожные заболевания, такие как атопический дерматит (АД), экзема, псориаз, витилиго, красная волчанка и другие, по праву можно отнести к группе сложных многофакторных заболеваний, в основе которых лежит генетическая предрасположенность. На возникновение и течение хронических дерматозов, помимо генетической предрасположенности, влияют следующие эпигенетические факторы: образ жизни и уровень стресса (оксидативный, физиологический, психологический), воздействие факторов окружающей среды (токсины, загрязняющие вещества, радиация), нутрициональные факторы (дефицит макро- и микронутриентов, в частности омега-3 ПНЖК, железа, витамина D), гормональные факторы и старение (возраст-ассоциированные изменения).
В течение последних десятилетий рацион современного человека претерпел значительные изменения, что отразилось на содержании в пищевых продуктах специфических компонентов, таких как омега-3 ПНЖК, витамин D, антиоксиданты, железо, фолаты, и это не могло не сказаться на глобальном росте аутоиммунных и аллергических заболеваний в обществе. В настоящее время в России у очень немногих людей питание может считаться сбалансированным. Повседневный рацион большинства россиян в XXI в. — высокоуглеводная и жирная пища с недостаточным количеством животного белка, дефицитом витаминов и микроэлементов.
Дефицит витамина D является новой неинфекционной пандемией XXI в. среди взрослых людей, проживающих севернее 35-й параллели, что обусловлено дефицитом инсоляции у жителей мегаполисов. Он патогенетически связан с ростом распространенности аутоиммунных заболеваний — сахарного диабета 1-го типа, ревматоидного артрита, атопического дерматита, гнездной алопеции, системной красной волчанки, псориаза и др. [2–7]. Жители всей территории России, Европы, практически всей Северной Америки попадают в зону риска дефицита/недостаточности витамина D, что неудивительно, так как угол падения УФ-лучей в этих регионах земного шара не позволяет полноценно использовать механизм синтеза витамина D в коже. Согласно данным многочисленных исследований, можно утверждать, что не менее 50% населения земного шара имеют в той или иной выраженности дефицит витамина D [8]. В группе риска находятся грудные младенцы, пожилые люди, люди с ограниченными возможностями пребывания на солнце, темнокожие, люди с ожирением, люди с заболеваниями, сопровождающимися нарушением всасывания жиров, в т.ч. перенесшие операции шунтирования желудка. С возрастом доля людей с дефицитом витамина D увеличивается до 80–90% [9].
В настоящее время витамин D рассматривается не только как гормон, регулирующий кальциевый гомеостаз и остеогенез, но и как фактор, участвующий в регуляции клеточной пролиферации и дифференцировке, апоптозе, иммуногенезе [10]. Доказано влияние витамина D на патогенез многих дерматозов, в особенности с аутоиммунным механизмом развития.
К центральным механизмам, лежащим в основе системных проявлений как псориаза, так и дефицита витамина D, относят низкоактивное генерализованное неспецифическое воспаление [11]. Под влиянием витамина D увеличивается синтез IL-10, подавляющего активность Thl-клеток, и снижаются уровни TNF-α и IFN-γ [12]. В исследованиях Бекировой Э.Ю. выявлено ингибирующее действие на синтез TNF-α мононуклеарными клетками витамина D [13]. В исследовании Peterson C.A., Heffernan M.E. доказана обратная корреляционная зависимость между сывороточными уровнями 25(OH)2D и уровнем TNF-α, что подтверждает противовоспалительные биологические эффекты витамина D [14].
По некоторым данным, кератиноциты содержат рецепторы к 1,25(OH)2D, в связи с чем активные метаболиты витамина D могут подавлять пролиферацию данных клеток [15]. Это послужило толчком для дальнейших исследований ассоциаций между аллельными вариантами рецептора витамина D (VDR) и псориазом [16]. Рецептор витамина D представляет собой лиганд-активированный продукт транскрипции, который опосредует геномные эффекты 1,25-дигидроксивитамина D в самых разнообразных тканях организма. Ген, кодирующий VDR, находится на хромосоме 12q и состоит из 11 экзонов, несущих генетическую информацию. В мировой литературе представлены данные о полиморфных вариантах гена VDR: во 2-м экзоне — FokI, BsmI, в 8-м интроне — ApaI, в 9-м экзоне — TaqI [17]. Halsall J. обнаружил ассоциацию между полиморфизмом промоторной зоны гена VDR и предрасположенностью к псориазу [18]. Таким образом, наличие у витамина D терапевтического эффекта при лечении псориаза обусловлено его иммуносупрессивным действием, подавлением пролиферации и стимуляцией дифференцировки кератиноцитов. Это позволяет рассмотреть ген VDR как вероятный ген псориаза [19].
На настоящий момент существуют как экспериментальные, так и клинические работы, демонстрирующие мощный антипролиферативный эффект витамина D в кератиноцитах эпидермиса, что может обеспечивать защиту кожи от некоторых видов рака, в т.ч. и наиболее злокачественной формы — меланомы.
Омега-3 ПНЖК
Значительное количество пищевых нутриентов уже имеют доказанное влияние на иммунные функции. Наиболее хорошо изучены в этом контексте полиненасыщенные жирные кислоты омега-3 (ПНЖК), которые используют в терапии хронических воспалительных заболеваний кожи — псориаза, атопического дерматита, акне, трофических язв и др. Они способствуют предотвращению и снижению воспалительных и аллергических процессов, в т.ч. при заболеваниях с нарушением в иммунном статусе.
В эстетической медицине омега-3 ПНЖК рекомендуют для профилактики преждевременного старения кожи, защиты от повреждений, связанных с инсоляцией. Омега-3 ПНЖК стимулируют рост и деление клеток, обеспечивают синтез коллагена, что позволяет бороться с морщинами, атрофией и ксерозом кожи.
Выявленные патогенетические изменения у больных псориазом показывают, что они нуждаются не только в медикаментозной, но и нутрицевтической поддержке. Эту необходимую поддержку обеспечивают омега-3 ПНЖК, являясь эссенциальными факторами питания [19–21]. Они незаменимы для нормального обмена веществ в организме человека. Доказано, что в результате проведения коррекции дефицита омега-3 ПНЖК у больных псориазом наблюдается положительный противовоспалительный эффект, уменьшается активность течения дерматоза и количество рецидивов заболевания. Важно отметить, что данная коррекция способствует нормализации показателей липидного обмена и повышению эффективности терапии в целом [22–26].
На сегодняшний день существует необходимая доказательная база, достаточная для утверждения, что каждый человек, проживающий в регионе с обедненным содержанием омега-3 ПНЖК в рационе (вся территория России), должен дополнительно принимать к пище препараты, содержащие ЭПК и ДГК для профилактики возраст-ассоциированных заболеваний, неинфекционных заболеваний, увеличения продолжительности и качества жизни.
Дефицит железа
Железо является эссенциальным биометаллом, играющим важную роль в функционировании всех клеток организма. Биологическое значение железа определяется его способностью обратимо окисляться и восстанавливаться, что обеспечивает его участие в процессах тканевого дыхания. При дефиците железа развивается состояние гипоксии во всем организме.
По данным ВОЗ, железодефицитное состояние диагностируется у 3,6 млрд человек, что превышает 1/3 часть всего населения нашей планеты, и бо´льшая часть из них — женщины и дети. Несбалансированное и недостаточное как в качественном, так и в количественном отношении питание привело к тому, что на территории России около 12% женщин фертильного возраста страдают ЖДА, а скрытый дефицит железа наблюдается почти у половины данной категории женщин. А по данным Минздравсоцразвития РФ, в России каждый третий ребенок и практически каждая беременная и кормящая женщина страдают ЖДА либо имеют латентный дефицит железа. Значительное влияние дефицита железа на психическое и физическое развитие, поведение и работоспособность делает его серьезной проблемой для здоровья общества. Со стороны кожного покрова сидеропения проявляется повышенной сухостью, замедлением регенерации кожи, тусклостью, ломкостью и замедленным ростом волос, ониходистрофией и койлонихией. Кроме этого, отмечается извращение вкуса и обоняния из-за развития эпителиопатии.
Восполнить дефицит железа без назначения лекарственных препаратов невозможно, однако поддержание его достаточного уровня в организме — задача грамотной диетической коррекции. Содержание железа в продуктах питания может быть достаточным, но его биодоступность невысока: не более 10% гемового и 1–1,5% негемового железа. Кроме того, усвоение железа сильно зависит от микроокружения пищи. Следовательно, использование продуктов питания, дополнительно обогащенных железом, является не только целесообразным, но и необходимым.
Заместительная гормональная терапия
Состояние кожи и ее производных (волос и ногтей) находится под влиянием целого ряда нейрогуморальных факторов, среди которых важную роль играют гормоны. Гормоны определяют толщину и рельеф эпидермиса, тип оволосения и свойства волос, секреторную активность сальных и потовых желез, состояние ногтей, кровоснабжение кожи и др. [27].
Основными половыми гормонами, обеспечивающими красоту и здоровье кожи, являются эстрогены, которые в физиологических концентрациях придают коже упругость, способствуют синтезу волокон зрелого коллагена, участвуют в регенерации, укрепляют дермо-эпидермальное соединение и регулируют функции сальных желез. Поэтому дефицит эстрогенов способен быстро приводить к увяданию и истончению кожи, повышению ее сухости и травматизации, что внешне будет проявляться в виде сетки мелких морщин и шелушения.
Однако для здоровья кожи и ее производных женщине необходимы не только эстрогены, но и прогестерон с тестостероном. Прогестерон тормозит синтез тропоколлагена в фибробластах соединительной ткани и оказывает незначительное стимулирующее действие на сальные железы, способствуя секреции кожного сала [28]. Сегодня есть данные об эффективности применения прогестерона при лечении угревой болезни у женщин, поскольку он тормозит биотрансформацию тестостерона в 5α-дигидротестостерон (5α-ДГТ) и конкурирует с 5α-ДГТ за андрогеновые рецепторы в волосяных фолликулах и сальных железах, снижая их активность.
Тестостерон регулирует интенсивность клеточного деления, процессы дифференциации, секреции и ороговения. Этот гормон придает коже мягкость, эластичность, упругость и влияет на бактерицидные функции кожи, которые зависят от уровня ее кровоснабжения и функционального состояния потовых и сальных желез. Под влиянием тестостерона кожа сохраняет необходимую увлажненность за счет формирования полноценного липидного барьера вследствие повышения активности сальных желез. Тестостерон также оказывает противовоспалительные эффекты, поскольку он подавляет действие протеолитических ферментов, связанных с деградацией коллагена. Тестостерон отвечает за синтез коллагена, миозина, актина и других мышечных белков, поэтому его роль в поддержании мышечного тонуса кожи является одной из ключевых [27].
Старение кожи является отражением всех гормональных нарушений, которые развиваются в связи с системным старением. К настоящему времени накоплен огромный доказательный базис для утверждения, что клинический дефицит половых гормонов (эстрогенов, прогестерона и тестостерона) у женщин является абсолютным показанием для назначения им заместительной гормональной терапии соответствующими гормонами. Такой подход позволяет укрепить женское здоровье и красоту изнутри, что одновременно способствует улучшению здоровья кожи, существенно повышая эффективность традиционных косметологических процедур.
Кроме того, при проведении исследования влияния ЗГТ на течение псориаза 2-го типа у женщин в постменопаузе было доказано, что дополнительное включение ЗГТ в состав комплексной терапии псориаза способствует повышению эффективности терапии с выраженной редукцией клинических симптомов и улучшением качества жизни и сопряжено с коррекцией гормонального статуса крови [29].
Заключение
Таким образом, к лечению дерматологического пациента нужно подходить комплексно, учитывая все эпигенетические факторы. Ведь, как уже говорилось выше, «генетика предполагает, а эпигенетика располагает». Поэтому, помимо назначения стандартной схемы лечения дерматоза, важно заниматься коррекцией нутрициональных и гормональных дефицитов. Особое значение имеет коррекция дефицита витамина D, омега-3 ПНЖК, железа и возраст-ассоциированного дефицита половых гормонов.
Хочется отметить линейку препаратов NFO (NFO Оmega-3; NFO Gentle Iron; NFO Vitamin D), зарекомендовавших себя как эффективные компоненты нутрицевтической поддержки. Важно понимать, что при устранении всех этих триггерных факторов у пациента будет наблюдаться более длительная ремиссия. Соответственно, комплексный подход к лечению пациента — ключ к успеху.